Страница: 2/9
Аморфное состояние образуется при быстром- (106 О С/с и более) охлаждении расплава. Например, при охлаждении ряда сплавов из жидкого состояния образуются так называемые металлические стекла, обладающие специфическими физико-механическими свойствами.
Атомы в кристаллическом твердом теле располагаются в пространстве закономерно, периодически повторяясь в трех измерениях через строго определенные расстояния, т. е. образуют кристаллическую решетку. Кристаллическую решетку можно «построить», выбрав для этого определенный «строи тельный блок» (аналогично постройке стены из кирпичей) и многократно смещая этот блок по трем, непараллельным направлениям. Такая «строительная» единица кристаллической решетки имеет форму параллелепипеда и называется элементарной ячейкой. Все элементарные ячейки, составляющие кристаллическую решетку, имеют одинаковую форму и объемы. Атомы могут располагаться как в вершинах элементарной ячейки, так и в других ее точках (в узлах кристаллической решетки). В первом случае элементарные ячейки называются простыми (примитивными), во втором — сложными. Если форма элементарной ячейки определена и известно расположение всех атомов внутри нее, то имеется полное геометрическое описание кристалла, т. е. известна его атомно-кристаллическая структура.
1.2. Энергетические условия процесса кристаллизации. Почему превращения происходят при строго определенных температурах?
Любое вещество, как известно, может находиться в трех агрегатных состояниях: газообразном, жидком и твердом. В чистых металлах при определенных температурах происходит изменение агрегатного стояния твердое состояние сменяется жидким при температуре плавления, жидкое состояние переходит в газообразное при температуре кипения. Температуры перехода зависят от давления но при постоянном давлении они вполне определенны.
При переходе из жидкого состояния в твердое образуется кристаллическая решетка, возникают кристаллы. Такой процесс называется кристаллизацией. Чем объясняется существование при одних температурах жидкого, а при других температурах твердого состояния и почему превращение происходит при строго определенных температурах?
В природе все самопроизвольно протекающие превращения, а следовательно, кристаллизация и плавление обусловлены тем, что новое состояние в новых условиях является энергетически более устойчивым, обладает меньшим запасом энергии.
Поясним примером. Тяжелый шарик из положения 1 (рис. 1) стремится попасть в более устойчивое положение 2, так как потенциальная энергия в положении 2 меньше, чем в положении 1.
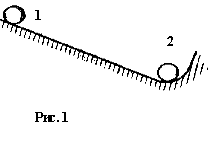 Энергетическое состояние системы, имеющей огромное число охваченных тепловым движением частиц (атомов, молекул), характеризуется особой термодинамической функцией F, называемой свободной энергией (свободная энергия F = U — ТS, где U — внутренняя энергия системы; Т— абсолютная температура; S—энтропия). Можно сказать, что чем больше свободная энергия системы, тем система менее устойчива, и если имеется возможность, то система переходит в состояние, где свободная энергия меньше («подобно» шарику, который скатывается из положения 1 в положение 2, если на пути нет препятствия).
Энергетическое состояние системы, имеющей огромное число охваченных тепловым движением частиц (атомов, молекул), характеризуется особой термодинамической функцией F, называемой свободной энергией (свободная энергия F = U — ТS, где U — внутренняя энергия системы; Т— абсолютная температура; S—энтропия). Можно сказать, что чем больше свободная энергия системы, тем система менее устойчива, и если имеется возможность, то система переходит в состояние, где свободная энергия меньше («подобно» шарику, который скатывается из положения 1 в положение 2, если на пути нет препятствия).
С изменением внешних условий, например температуры, свободная энергия системы изменяется по сложному закону, но различно для жидкого и кристаллического состояний. Схематически характер изменения свободной энергии жидкого и твердого состояний с температурой показан на рис. 2
Выше температуры Тs, меньшей свободной энергией обладает вещество в жидком состоянии, ниже Тs — вещество в твердом состоянии. Следовательно, выше Ts, вещество должно находиться в жидком состоянии, а ниже Тs, — в твердом, кристаллическом.
Очевидно, что при температуре, равной Ts, свободные энергии жидкого и твердого состояний равны, металл в обоих состояниях находится в равновесии. Эта температура Ts и есть равновесная или теоретическая температура кристаллизации.
Реферат опубликован: 5/05/2007